متادون برنامه ریزی شده نیاز کلی به مواد مخدری را پس از فیوژن خلفی ستون فقرات کودکان کاهش می دهد: یک سری مطالعه تک مرکزی گذشته نگر
خلاصه
زمینه
فیوژن خلفی ستون فقرات برای اصلاح اسکولیوز ایدیوپاتیک نوجوانان با درد قابل توجهی پس از عمل همراه است. روش های مختلف به عنوان بخشی از یک طرح ضد درد چندوجهی گزارش شده است. متادون داخل وریدی به عنوان یک آگونیست مو-اپیوئید و آنتاگونیست N-متیل-D-آسپارتات (NMDA) عمل می کند و نشان داده شده است که اثرات حفظ کننده مواد مخدر دارد. رویکرد چندوجهی ما شامل بیدردی کنترلشده توسط بیمار هیدرومورفونی (PCA) با و بدون متادون قبل از برش جراحی ، و اخیراً متادون پس از عمل بدون PCA است.
اهداف
ما فرض کردیم که پروتکلی شامل دوزهای متادون برنامه ریزی شده پس از عمل، مصرف مواد مخدری را در مقایسه با استراتژی مبتنی بر PCA کاهش می دهد.
مواد و روش ها
یک مرور نمودار گذشته نگر از بیماران تحت فیوژن خلفی ستون فقرات برای اسکولیوز ایدیوپاتیک نوجوان بین سالهای 2015 و 2020 انجام شد. سه گروه بیمار وجود داشت: گروه PCA یک هیدرومورفون PCA بدون متادون دریافت کرد ، گروه PCA + متادون متادون قبل از برش جراحی preincisional و هیدرومورفون PCA دریافت کرد ، گروه متادونی متادون قبل از برش جراحی دریافت می کنند ، متادون برنامهریزیشده پس از عمل و بدون PCA دریافت کرد. پیامد اولیه مصرف مواد مخدری بعد از عمل بیش از 72 ساعت بود. پیامدهای ثانویه شامل نمرات درد، نمرات آرامبخشی و مدت اقامت بود.
نتایج
گروه PCA (n = 26) 0.33 میلی گرم بر کیلوگرم (95٪ CI [0.28، 0.38]) معادل کل هیدرومورفون، گروه PCA + متادون (n = 39) 0.30 میلی گرم بر کیلوگرم (925٪، 38) [0. معادلهای هیدرومورفون، و متادون گروهی (22=n) 0.18 میلیگرم بر کیلوگرم (95% فاصله اطمینان (CI [0.15، 0.21]) کل معادلهای هیدرومورفون (0.00096 = p). هیچ تفاوت آماری معنی داری بین گروه ها برای پیامدهای ثانویه وجود نداشت.
نتیجه
پروتکلی با دوزهای متادون حین عمل و برنامه ریزی شده بعد از عمل باعث کاهش 45 درصدی مصرف مواد مخدری در مقایسه با پروتکل مبتنی بر PCA با بی دردی مشابه پس از فیوژن خلفی ستون فقرات در کودکان شد
1. مقدمه
فیوژن ستون فقرات خلفی برای اصلاح اسکولیوز ایدیوپاتیک نوجوانان (AIS) با درد قابل توجه بعد از عمل همراه است. 1 پروتکل های ضد درد پس از عمل متعددی گزارش شده است، از جمله بی حس کننده های موضعی اپیدورال، اپیوئیدهای داخل نخاعی، و مواد مخدری سیستمیک از طریق بی دردی کنترل شده توسط بیمار (PCA)، که همگی دارای واریس هستند. سطوح شواهد.2 بسیاری از این روش ها با معایب قابل توجهی از جمله ضعف حرکتی ناشی از بی دردی اپیدورال که معاینه عصبی بعد از عمل را مخدوش می کند یا میزان بالای خارش ناشی از مواد مخدری داخل نخاعی همراه است. استفراغ، افسردگی تنفسی و طولانی شدن بازگشت عملکرد روده، اکثر پروتکل های بی دردی پس از عمل سعی می کنند از یک رویکرد چندوجهی برای کاهش نیاز به داروهای مخدر استفاده کنند. متادون داخل وریدی یک شبه مخدری منحصر به فرد است که روی گیرنده های متعددی از جمله مو-اپیوئید، کاپا-افیون، N-متیل-D-آسپارتات (NMDA)، سروتونین و نوراپی نفرین اثر می کند. شواهد نشان میدهد که متادون در صورتی که قبل از برش برای فیوژن خلفی ستون فقرات و روشهای Nuss داده شود، یک اثر کلی محافظت از مواد مخدری ایجاد میکند. تصور میشود که این اثر به دلیل عملکرد متادون در چندین مکان گیرنده مختلف در سیستم عصبی مرکزی باشد که تعدیل میکنند. مسیرهای صعودی درد و تغییر ادراک و پاسخ به درد.
در سال 2015، موسسه ما یک گروه چند رشته ای ایجاد کرد تا یک مسیر بهبودی پیشرفته پس از همجوشی ستون فقرات ایجاد کند. این کار بر اساس نتایج حاصل از سایر بیمارستانهای کودکان است که مسیرهای بهبودی بهبودیافته را اجرا میکنند، با هدف مدت اقامت کوتاهتر و کنترل بهتر درد. مانیتورینگ) به جای بخش مراقبت های ویژه و بسیج تهاجمی تر و زودهنگام با فیزیوتراپی. علاوه بر این، کمیته تصمیم گرفت که از کاتترهای اپیدورال که در عمل جراحی قرار داده شده اند، فاصله گرفته و یک پروتکل مبتنی بر PCA ایجاد کند. رویکرد اولیه شامل هیدرومورفون PCA با افزودن متادون پیش از برش بود. اخیراً، به دلیل کمبود مواد مخدری داخل وریدی که ما را بر آن داشت تا ضایعات دارویی ناشی از PCA را به حداقل برسانیم، و همچنین اثرات بالینی مثبتی که با متادون پیش از برش مشخص شد، پروتکل خود را اصلاح کردیم تا دوزهای برنامهریزی شده بعد از عمل متادون را به همراه پرو ناتا (PRN) شامل شود. هیدرومورفون IV به جای PCA.
ما یک بررسی نمودار گذشته نگر از همه بیمارانی که تحت فیوژن خلفی ستون فقرات برای AIS در موسسه ما قرار گرفتند، انجام دادیم. نتیجه اولیه مصرف مواد مخدری بعد از عمل در 72 ساعت اول پس از جراحی بود. پیامدهای ثانویه شامل نمرات درد همراه با فعالیت، امتیازات آرامبخشی، استفاده از بنزودیازپین (دیازپام)، مدت اقامت و تعداد مطلق دوزهای هیدرومورفون PRN IV بود. فرضیه ما این بود که پروتکلی بر اساس دوزهای متادون برنامه ریزی شده در مقایسه با استراتژی مبتنی بر PCA منجر به کاهش مصرف کلی مواد مخدری می شود.
2 روش
این مطالعه در سال 2019 توسط هیئت بررسی نهادی علوم بهداشتی دانشگاه ویسکانسین برای بررسی گذشته نگر تأیید شد. برنامه های جراحی از ژوئن 2015 تا فوریه 2020 برای شناسایی بیماران کودکان تحت فیوژن خلفی ستون فقرات برای AIS توسط تیم جراحی ارتوپدی اطفال ما بررسی شد. بیماران در صورت تشخیص اسکولیوز عصبی عضلانی یا مادرزادی از مطالعه حذف شدند.
بیماران بر اساس پروتکل در زمان عمل به سه گروه درمانی (PCA گروهی، گروهی PCA + متادون، گروهی متادون) تقسیم شدند. مدیریت بیهوشی حین عمل شامل یک بیهوشی کامل داخل وریدی با پروپوفول برای تسهیل نظارت عصبی بود. بیماران در گروههای PCA و PCA-+-متادون یک انفوزیون مواد مخدری حین عمل (فنتانیل یا رمی فنتانیل) با مواد مخدری pro renata (PRN) در طول مورد در صورت صلاحدید دریافت کردند. دگزامتازون و اندانسترون برای پیشگیری از تهوع و استفراغ بعد از عمل تجویز شد.
دوره مطالعه روزهای 0 تا 3 بستری در بیمارستان بود. نمرات درد پس از عمل با فعالیت (مقیاس رتبهبندی عددی 0-10) هر 8 ساعت ثبت شد و میانگین برای هر روز محاسبه شد. .
داده های دارویی، از جمله کل مواد مخدری (متادون، هیدرومورفون، اکسی کدون، مورفین، مورفین با رهش طولانی) استفاده از همه منابع (IV، PO، PCA) و دوزهای دیازپام جمع آوری شد. اپیوئیدهای کوتاه اثر (فنتانیل، رمی فنتانیل، آلفنتانیل، سوفنتانیل)، که در حین عمل به صورت بولوس یا انفوزیون تجویز میشوند، از مجموع مواد مخدری ما حذف شدند. تمام مصرف مواد مخدری با استفاده از فاکتورهای تبدیل زیر به معادل های هیدرومورفون تبدیل شد: 1 میلی گرم هیدرومورفون وریدی = 5 میلی گرم مورفین وریدی = 15 میلی گرم مورفین PO = 10 میلی گرم اکسی کدون PO = 5 میلی گرم متادون IV.13-16
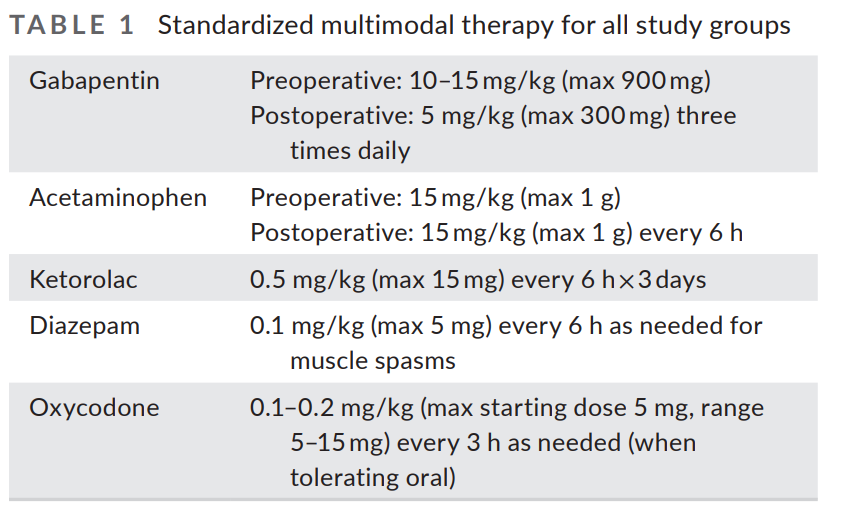
در دوره بعد از عمل، همه بیماران بهبود می یابند درمان استاندارد چندوجهی شامل گاباپنتین، استامینوفن، و داروهای ضد التهابی غیر استروئیدی را دریافت کرد (جدول 1)
TABLE 1. Standardized multimodal therapy for all study groups
Gabapentin | Preoperative: 10–15 mg/kg (max 900 mg) Postoperative: 5 mg/kg (max 300 mg) three times daily |
Acetaminophen | Preoperative: 15 mg/kg (max 1 g) Postoperative: 15 mg/kg (max 1 g) every 6 h |
Ketorolac | 0.5 mg/kg (max 15 mg) every 6 h × 3 days |
Diazepam | 0.1 mg/kg (max 5 mg) every 6 h as needed for muscle spasms |
Oxycodone | 0.1–0.2 mg/kg (max starting dose 5 mg, range 5–15 mg) every 3 h as needed (when tolerating oral) |
roup PCA، تقریباً از ژوئن 2015 تا ژوئن 2016، یک هیدرومورفون PCA را بدون هیچ گونه متادون حین عمل دریافت کرد. هیدرومورفون PCA به صورت 4 میکروگرم بر کیلوگرم (حداکثر 0.2 میلی گرم) هر 8 دقیقه با دوز تقاضای پرستاری 8 میکروگرم بر کیلوگرم (حداکثر 0.4 میلی گرم) هر ساعت سفارش داده شد. PCA ها نرخ پایه یک شبه (2100-0600) 4 میکروگرم بر کیلوگرم در ساعت (حداکثر 0.2 میلی گرم در ساعت) برای شب اول و گزینه ای برای نرخ پایه یک شبه در شب دوم به صلاحدید تیم خدمات درد حاد داشتند. اگر احساس کردند کنترل درد بیمار در روز بعد از عمل ناکافی است (POD) 1. هدف این بود که هر بیمار از PCA به اکسی کدون خوراکی (مصرف مایعات کامل یا رژیم غذایی عمومی) توسط POD 2 منتقل شود. داروهای خوراکی، آنها همچنین مورفین خوراکی با رهش طولانی مدت 15 میلی گرم دو بار در روز با اولین دوز موجود در بعد از ظهر POD1 تا زمان ترخیص دریافت کردند.
گروه PCA + متادون، از ژوئن 2016 تا نوامبر 2018، متادون IV پیش از برش 0.2 میلی گرم بر کیلوگرم (حداکثر 20 میلی گرم) و هیدرومورفون PCA دریافت کردند. هیدرومورفون PCA به صورت 4 میکروگرم بر کیلوگرم (حداکثر 0.2 میلی گرم) هر 8 دقیقه، با دوز تقاضای پرستاری 8 میکروگرم بر کیلوگرم (حداکثر 0.4 میلی گرم) هر ساعت سفارش داده شد. نرخ پایه برای بیمارانی که به 2 دوز تقاضا در ساعت یا بولوس های متعدد توسط پرستار در 3 ساعت متوالی نیاز داشتند، در دسترس بود. اگر بیماران PCA را به داروهای خوراکی تغییر داده بودند، این بیماران مورفین طولانی رهش 15 میلیگرم را دو بار در روز با اولین دوز در بعد از ظهر POD1 تا زمان ترخیص دریافت کردند.
متادون گروهی، از نوامبر 2018 تا فوریه 2020، متادون پیش از برش 0.2 میلی گرم بر کیلوگرم (حداکثر 20 میلی گرم)، متادون 0.1 میلی گرم بر کیلوگرم (حداکثر 5 میلی گرم) IV در واحد مراقبت پس از بیهوشی (PACU) در اولین درخواست برای بی دردی، و متادون دریافت کرد. 0.1 میلی گرم بر کیلوگرم (حداکثر 5 میلی گرم) IV 6 ساعت پس از دوز PACU. در مارس 2019، بر اساس بازخورد فیزیوتراپیست های ما که رگرسیون عملکردی قابل توجهی را در POD2 در مقایسه با POD1 ذکر کردند، بیماران یک دوز اضافی متادون 0.1 میلی گرم بر کیلوگرم (حداکثر 5 میلی گرم) IV در عصر برنامه ریزی شده در سال 2000 در POD1 دریافت کردند (15=n). /22). دوزهای برنامه ریزی شده متادون برای نمرات آرامبخشی بیشتر یا مساوی 3 (در مقیاس 5 درجه ای) نگه داشته شدند. این گروه هیدرومورفون IV 5-10 میکروگرم بر کیلوگرم (حداکثر 0.2-0.4 میلی گرم) در صورت نیاز به صورت ساعتی در دسترس داشتند.
2.1 تکنیک جراحی
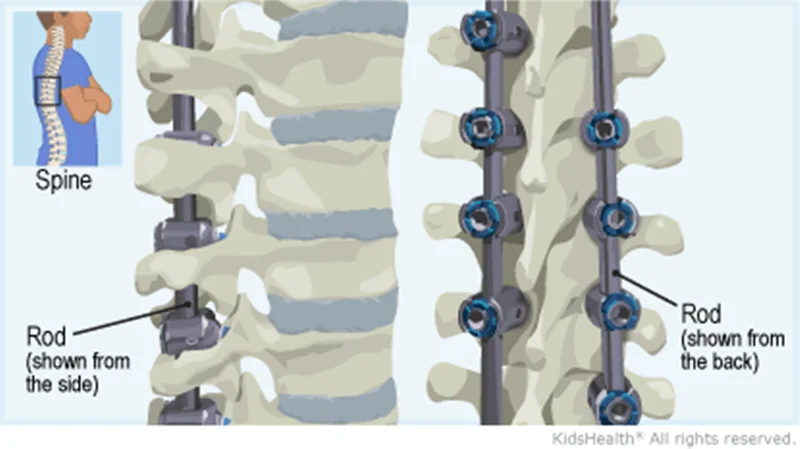
پس از اتمام زمان پیشبرشی مناسب، یک برش طولی از طریق پوست و بافت زیر جلدی انجام شد. ستون فقرات به صورت زیر پریوست در سطوح مناسب برای همجوشی قرار گرفت. با استفاده از انواع سیستم های هدایت رادیولوژیک (فلوروسکوپی، سی تی اسکن یا ناوبری)، ایمپلنت ها به صورت استراتژیک در محدوده محل همجوشی قرار گرفتند. سپس ستون فقرات با انواع مانورهای مکانیکی اصلاح شد. تصویربرداری نهایی تصحیح مناسب را مستند کرد. مانیتورینگ عصبی (MEPs و SSEPs) در طول روش برای اطمینان از اصلاح ایمن انحنا انجام شد. پیوند استخوان اهداکننده در اطراف ایمپلنت ها قرار داده شد و فاسیا، بافت زیر جلدی و پوست به روش استاندارد بسته شد. کل زمان جراحی برای همجوشی ستون فقرات خلفی (4 تا 7 ساعت) با توجه به عوامل مختلف، از جمله اندازه منحنی، اندازه بیمار، سفتی تغییر شکل و سایر عوامل نامشهود متفاوت بود.
2.2 تجزیه و تحلیل آماری
پیامد اولیه این مطالعه مصرف کلی مواد مخدطی روزهای 0-3 بود. معادل های هیدرومورفون و مدت اقامت با استفاده از آنالیز واریانس یک طرفه و به دنبال آن تست های تعقیبی Tukey HSD در صورت لزوم مقایسه شد. مقیاسهای درد و آرامبخشی بین گروهها با استفاده از آزمون کروسکال-والیس مقایسه شد. از دست دادن نمره درد و آرامبخش برای بیمارانی که قبل از ارزیابی POD3 ترخیص شده اند (درد: n = 2 از گروه PCA + متادون، n = 2 از متادون گروه، آرامبخش: n = 1 از گروه PCA، n = 2 از گروه PCA + متادون، n = 2 از متادون گروه) با استفاده از امتیازات POD0 تا POD2 با استفاده از موش های بسته R نسبت داده شد. 17 تعداد دوزهای دیازپام با رگرسیون دو جمله ای منفی مقایسه شد. معنی داری آماری به صورت p < .05 تعریف شد. تمامی تجزیه و تحلیل های آماری از نسخه R 3.5.2 استفاده کردند.
3 نتیجه
ما در مجموع 94 بیمار را شناسایی کردیم که بین ژوئن 2015 و فوریه 2020 توسط همان جراح ارتوپد اطفال تحت فیوژن خلفی ستون فقرات برای AIS قرار گرفتند. هشتاد و هفت بیمار معیارهای ورود ما را داشتند. هیچ بیمار در دوره قبل از عمل اپیوئید مصرف نمی کرد. سه بیمار در گروه PCA به دلیل داشتن یک کاتتر اپیدورال پس از عمل، که در سال 2015 در حال انتقال به پروتکل مبتنی بر PCA بودیم، از مطالعه خارج شدند. . یک بیمار به دلیل اینکه دچار بلوک کامل قلب حین عمل شده بود (PCA گروهی) که منجر به بستری طولانی مدت در بیمارستان شد، از مطالعه خارج شد. یک بیمار به دلیل آسیب نخاعی حین عمل (متادون گروهی) که منجر به بستری طولانی مدت در بیمارستان شد، از مطالعه خارج شد. جمعیت شناسی بیمار در بین گروه ها مشابه بود
طول مدت بستری در بیمارستان تفاوت معنی داری نداشت (جدول 2)
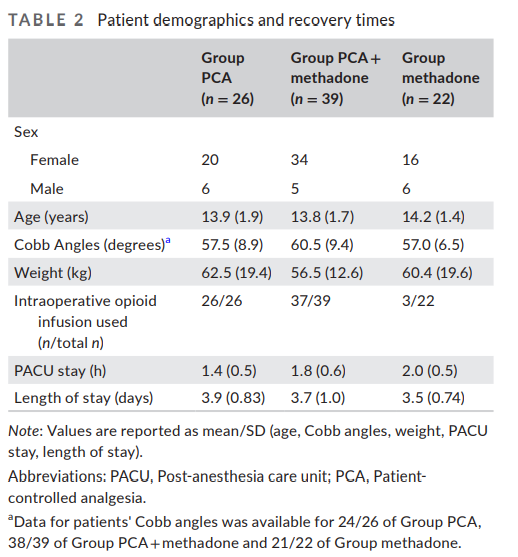
نتیجه اولیه ما از مصرف کل مواد مخدری بیش از POD 0-3 در شکل 1 نشان داده شده است. متادون گروهی نسبت به هر دو گروه PCA یا PCA + متادون به میزان قابل توجهی از مواد مخدری کمتری استفاده کرد (F[2,84] = 7.56, p = 0.00096؛ post-hoc مقایسه توکی: p = 0.73 برای PCA در مقابل متادون PCA + ، p =.0014 برای PCA در مقابل متادون، 0.0048 = p برای PCA + متادون در مقابل متادون) (جدول 3). متادون گروهی (بدون PCA) از میانگین (IQR) 2 (0.75، 5.25) دوز هیدرومورفون PRN IV قبل از انتقال به اکسی کدون PO استفاده کرد. 21 بیمار از 22 بیمار در این گروه PO oxycodone توسط POD2 مصرف می کردند
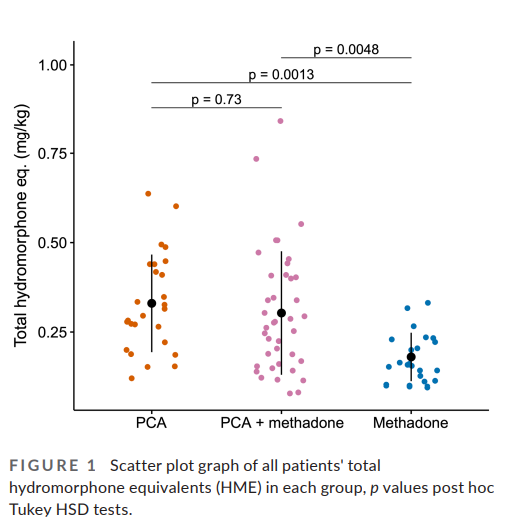
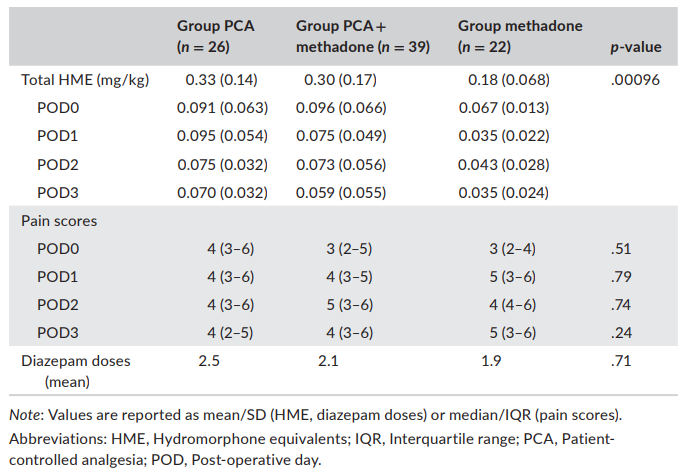
برای پیامدهای ثانویه، تفاوت معنیداری بین نمرات درد با میزان فعالیت، مصرف دیازپام یا نمره آرامبخشی وجود نداشت (جدول 3). میانگین نمرات آرامبخشی در همه گروه ها زیر 2 بود. با این حال، سه بیمار در گروه متادون دوز متادون شبانه POD0 را به دلیل نمره آرامبخشی 3 داشتند. زمان سپری شده در PACU در گروههای PCA + متادون و متادون در مقایسه با PCA طولانیتر بود (F[2,84] = 7.06، p. = 0.0015؛ مقایسات بعد از توکی: p = 0.040 برای PCA در مقابل متادون PCA + ، p =.0011 برای PCA در مقابل متادون، p = 0.22 برای PCA + متادون در مقابل متادون؛ جدول 2). هیچ یک از بیماران گروه متادون در 24 ساعت اول بعد از عمل، طولانی شدن QT را در حین تله متری تجربه نکردند.4. بحث
در این مطالعه گذشتهنگر که روشهای ضددردی مختلف را برای فیوژن خلفی ستون فقرات مقایسه میکند، نشان دادیم که یک پروتکل مبتنی بر متادون منجر به کاهش کلی مصرف مواد مخدری در طول 72 ساعت اول دوره پس از عمل میشود. بیماران گروه متادون در مقایسه با یک رژیم مبتنی بر PCA، تقریباً نصف مقدار مواد مخدری مصرف کردند، در حالی که نمرات درد معادل را حفظ کردند.
دستیابی به بی دردی معادل با نیازهای تجمعی به میزان قابل توجهی کمتر از نظر بالینی مهم است زیرا عوارض جانبی نامطلوب مواد مخدری با افزایش دوز تجمعی مواد مخدری همراه است. خدمات درد (APS). پس از چند ماه اول ایجاد این تغییر، APS مؤسسهای ما دیگر به طور معمول این بیماران را بررسی یا مشورت نکرد، زیرا مداخلات بیشتر ضروری نبود.
متادون داخل وریدی هم به عنوان آگونیست مو-مخدری و هم به عنوان آنتاگونیست NMDA عمل می کند و شواهد نشان داده است که اگر قبل از برش داده شود، اثر کلی محافظت از مواد مخدری را نشان می دهد. 1، 5 متادون همچنین بازجذب سروتونین و نوراپی نفرین را در مغز مهار می کند، که ممکن است به طور بالقوه باعث ایجاد آن شود. این یک اثر مخدری جایگزین با نیمه عمر حذف طولانی 24 تا 36 ساعت در دوزهای بالاتر است، اما پس از تجویز اولیه بولوس به سرعت در معرض توزیع مجدد قرار می گیرد و احتمالاً باعث ایجاد غلظت ناکافی در پلاسما برای بی دردی پس از مصرف کمتر می شود. mg/kg 0.1) و دوزهای یکبار مصرف. مدت بالینی اثر وابسته به دوز است و با تکرار دوز به طور قابل توجهی افزایش می یابد. 18، 19
فارماکوکینتیک متادون در نوجوانانی که تحت فیوژن خلفی ستون فقرات قرار می گیرند در مطالعات متعدد اندازه گیری شده است. 6، 18، 20 Stemland و همکاران. 0.25 میلی گرم بر کیلوگرم متادون وریدی قبل از برش جراحی در 17 بیمار تجویز شد و تخمین پارامترهای فارماکوکینتیک مشابهی را برای بزرگسالان یافت. آنها گزارش کردند که متادون پس از تجویز بولوس به سرعت در معرض توزیع مجدد قرار می گیرد و توصیه کردند که دوز قبل از برش را با انفوزیون حین عمل برای حفظ سطوح پلاسمایی ضد درد تجویز کنند. سطوح پس از توزیع مجدد تجویز به درخواست بیمار در دوران نقاهت مزیت دیگری دارد که امکان ارزیابی سطح آرام بخشی را قبل از دادن تریاک بیشتر فراهم می کند. شارما و همکاران 20 همچنین فارماکوکینتیک متادون بعد از عمل را در نوجوانان بررسی کردند و دریافتند که آنها در محدوده دوز 0.1-0.3 میلی گرم بر کیلوگرم خطی هستند. آنها اثر وابسته به دوز متادون را بر نمرات درد پس از عمل یا مصرف مواد مخدری پیدا نکردند، اما طرح مطالعه برای این پیامدهای ثانویه مورد استفاده قرار نگرفت. نویسندگان خاطرنشان کردند که، «علیرغم عدم وجود اثرات کمی خاص ضددرد و حفظ مواد مخدری متادون، تفاوتهایی در بیمارانی که متادون دریافت میکردند، به وضوح قابل مشاهده بود، هرچند حکایتی. پرستاران اتاق ریکاوری به طور خود به خود در مورد راحتی بیشتر در بیمارانی که در این تحقیق ثبت نام کرده بودند اظهار نظر کردند.» 20 فارماکوکینتیک پیچیده متادون، از جمله خطرات مرتبط با دوزهای مکرر، آن را به یک کاندیدای ضعیف برای تجویز PCA تبدیل می کند. با این حال، ممکن است نقشی برای دوزهای اضافی متادون در صورت نیاز در دوره پس از عمل وجود داشته باشد
یه و همکاران در پروتکل خود از دوز پیش برش کوچکتر اما دوز متادون پس از عمل مشابه استفاده کردند. آنها تقریباً 30٪ کاهش در کل مصرف مواد مخدری را در مقایسه با کنترل های تاریخی با مورفین داخل نخاعی و یک PCA مورفین نشان دادند، مشابه نتایج ما. They همچنین به مزایای هزینه مرتبط با حذف مواد مخدری PCA اشاره کرد. اخیراً، همان گروه دادههای فارماکوکینتیکی را برای این رژیم در جمعیت مختلط فیوژن خلفی ستون فقرات و ترمیم پکتوس اکاواتوم منتشر کرد. اگرچه بیماران سطوح پلاسمایی متادون کمتری نسبت به آنچه قبلاً گزارش شده بود داشتند. نتایج بالینی موثر برای بیدردی، شامل نمرات کمتر درد و مصرف کمتر مواد مخدری نسبت به گروههای کنترل تاریخی بود. هیچ موردی از افسردگی تنفسی یا طولانی شدن QTc در نمونه 38 بیمار آنها مشاهده نشد. مارتین و همکاران یک مطالعه آیندهنگر، تصادفی و کور بر روی 60 بیمار مبتلا به AIS، که برای فیوژن خلفی ستون فقرات مراجعه میکردند، برای دریافت انفوزیون رمی فنتانیل حین عمل به تنهایی، رمی فنتانیل به همراه متادون (0.1 میلیگرم بر کیلوگرم)، یا رمی فنتانیل به همراه منیزیم (50 میلیگرم/کیلوگرم بولوس) انجام داد. 10 mg/kg/h انفوزیون). آنها دریافتند کل نیاز به مواد مخدری (هیدرومورفون) در گروه رمی فنتانیل به تنهایی 0.11±0.34 میلی گرم بر کیلوگرم در مقایسه با 0.10±0.26 میلی گرم بر کیلوگرم در گروه متادون (0.035 = p) است، مشابه یافته های ما، که دوباره نشان می دهد استفاده از آن. متادون می تواند باعث کاهش کلی نیاز به مواد مخدری شود
ما از یک تخمین محافظه کارانه (5:1) برای تبدیل متادون به هیدرومورفون استفاده کردیم، بنابراین تفاوت بین گروه ها ممکن است بیشتر دست کم گرفته شود. (بنابراین 5:1 متادون:هیدرومورفون) ممکن است دقیق تر باشد، و ما تبدیل متادون خود را بر این شواهد بنا نهادیم تا تخمین محافظه کارانه تری نسبت به نسبت 7:1 مورفین: هیدرومورفون گزارش شده در سایر مطالعات (یعنی، ما متادون میلی گرم را تقسیم کنیم). /کیلوگرم 5 به جای 7 برای محاسبه HME). 15، 16، 20 از آنجایی که ما در حال بررسی استفاده از مواد مخدری بعد از عمل بودیم، مواد مخدری کوتاه اثر که در حین عمل به صورت بولوس یا انفوزیون تجویز می شدند، از مجموع مواد مخدری ما حذف شدند، در حالی که متادون پیش از برش در مجموع گنجانده شد. به دلیل مدت زمان طولانی اثر آن، کل می شود. به جز سه بیمار در گروه متادون، انفوزیون مواد مخدری حین عمل عمدتاً در گروههای PCA و PCA + متادون مورد استفاده قرار گرفت و به استثنای دوزهای حین عمل ممکن است دوز کلی مواد مخدری حین عمل دست کم گرفته شود.
علاوه بر نمرات درد مشابه بین همه گروهها، گروه متادون چند دوز، نمرات آرامبخشی و مدت اقامت مشابهی داشتند. طول مدت اقامت توسط عوامل بسیاری تعیین می شود و با اجرای پروتکل بهبودی بهبود یافته ما که در ابتدای دوره مطالعه ما در سال 2015 ایجاد شد، از میانگین تقریباً 5 روز به 3 روز کاهش یافت. این پروتکل شامل آموزش گسترده قبل از عمل، بعد از عمل بود. پذیرش در بخش مراقبت های عمومی به جای بخش مراقبت های ویژه (ICU) و بسیج تهاجمی و فیزیوتراپی. پس از بهینه سازی سایر جنبه های مدیریت پس از عمل، نشان دادن مزیت بیشتر به دلیل کاهش مواد مخدری دشوار بود. 8-10
محدودیتهای متعددی برای بررسی گذشتهنگر ما وجود دارد، از جمله دادههای ناقص و ارزیابهای متغیر (کارکنان پرستاری) برای ارزیابی درد و تصمیمگیری برای تجویز داروهای PRN. مطالعه ما نیز با حجم نمونه کوچک و نابرابر در سه گروه محدود شده است. اگرچه ما یک موسسه نسبتا کوچک هستیم، اما توانستیم تقریباً همه بیمارانی را که تحت فیوژن خلفی ستون فقرات قرار میگیرند، بگیریم، و هدف ما مقایسه یک نمونه مداوم از بیماران در طول تغییرات پروتکل بود. وزن واقعی بدن برای محاسبات مورد استفاده قرار گرفت، اما ارائه دهندگان ممکن است دوزهای نزدیک به وزن بدن ایده آل برای نوجوانان چاق داشته باشند. میانگین وزن در بین گروه ها تفاوت معنی داری نداشت. در نهایت، به دلیل تغییرات پروتکل که شامل اندانسترون برنامه ریزی شده پس از عمل در گروه متادون بود، نتوانستیم بررسی کنیم که آیا استفاده از ضد استفراغ در بین گروه ها متفاوت است یا خیر. این تغییر برای کاهش تنوع پرستاری در تجویز داروهای ضد استفراغ PRN اعمال شد. Sadhasivam و همکاران 18 در مطالعه خود در مورد بررسی چند دوز متادون در کودکانی که تحت عمل فیوژن خلفی ستون فقرات و ترمیم پکتوس اکاواتوم قرار گرفتند، دریافتند که بروز تهوع و استفراغ (PONV) پس از عمل به طور مثبت با دوز تجمعی مواد مخدری مرتبط است، بنابراین بعید به نظر میرسد که افزایش در آن افزایش یابد. PONV در گروه متادون ما در مقایسه با گروه های PCA.
5 نتیجه گیری
برای کودکانی که تحت فیوژن خلفی ستون فقرات قرار میگیرند، یک پروتکل ضد درد چندوجهی شامل دوزهای متادون داخل وریدی حین عمل و بعد از عمل، در مقایسه با PCA با یا بدون متادون قبل از برش، در مصرف کلی مواد مخدری 44 درصد کاهش مییابد، بدون اینکه بیدردی را به خطر بیندازد
hydromorphone equivalents using the following conversion factors: 1 mg of IV hydromorphone = 5 mg of IV morphine = 15 mg PO morphine = 10 mg PO oxycodone = 5 mg IV methadone.
برگرفته از :
Pediatric Anesthesia Journal
https://onlinelibrary.wiley.com/doi/10.1111/pan.14526



دیدگاه خود را بنویسید